化工学院化学生物学团队在白血病新靶标发现-抗癌药研发-分子标志物确认一体化研究方面取得系列进展,发现了慢性粒细胞白血病(CML)的新的治疗靶标,研发了针对该靶标的抗癌先导药物,并逆转了BCR-ABL非依赖型激酶抑制剂(TKIs)耐药。这一系列研究整合了化学的研究思想与生物学前沿技术,着眼于临床医学领域的关键科学问题,攻克了白血病治疗领域抗药性难题,属于转化医学的开拓性研究,也是我校在医工交叉领域取得的又一重要成果。张志超教授的化学生物学研究团队始终致力于研发Bcl-2蛋白的靶向抗癌药物,在2020年首先发现Hsp70蛋白能够作为类Bcl-2蛋白,与经典Bcl-2家族协同促进肿瘤发生的功能。该成果已经发表于自然指数(Nature Index)收录的82种全球顶级期刊之一(J Bio Chem.,2020,295, 12900)。以此为基础,该研究的通讯作者宋婷副教授提出假说,综合运用化学和生物学多学科技术手段,迅速从该团队已经创制的Bcl-2抑制剂分子库中筛选获得了首个特异性的Hsp70/Bim小分子抑制剂S1g-2,成为新的抗癌候选药物。相关成果由王紫千副教授发表于医学大类Q1杂志Eur J Med Chem.,2021,220, 113452.
接下来,该团队进一步针对TKI耐药的白血病开展转化医学和创新药物研究。虽然“神药”格列卫革命性地提高了白血病患者的生存期,但是约20%-30%的患者对其产生耐药,其中部分患者的细胞能够通过不依赖BCR-ABL激酶调控的耐药机制产生逃逸,成为目前治疗白血病的最大难题。发现新的肿瘤靶标是白血病等BCR-ABL阳性肿瘤的基础研究和靶向药物研发的核心和关键。
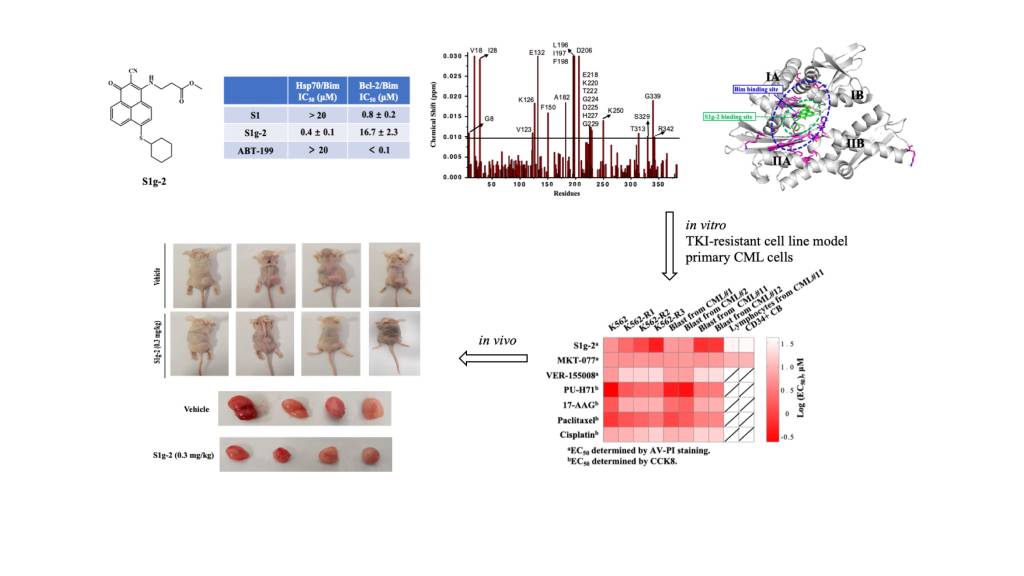
首个靶向Hsp70/Bim的小分子抑制剂S1g-2在TKIs耐药的CML细胞和小鼠移植瘤模型中表现出高效低毒的抗肿瘤活性
通过多次实验,该团队发现S1g-2杀伤TKIs耐药的白血病细胞的趋势完全相反于所有已知的Hsp70抑制剂。进一步,该团队通过化学生物学、结构生物学、细胞生物学、生物信息学等多种研究方法,全面系统地揭示了Hsp70/Bim调控白血病细胞逃避1-3代“神药”的分子机制,证明S1g-2在细胞水平和动物体内具有高效低毒的抗白血病活性,和逆转BCR-ABL非依赖性TKIs耐药的作用,为白血病治疗提供了全新机制、全新结构的抗癌先导化合物。相关成果由宋婷副教授发表于Nature旗下杂志Leukemia。Leukemia是美国白血病学会会刊,在血液病学期刊中排名第3,在肿瘤学期刊中排名第9。
该研究得到了国家自然科学基金及大连理工大学-辽宁省肿瘤医院医工合作项目的资助。
文章链接: